Stj.Dr. Emine Ataç, Prof.Dr.Ahmet Dobrucalı
Pankreas karın içinde midenin arkasında yer alan yumuşak kıvamda ve yassı uzun şekilde bir organımızdır. Başlıca görevi sindirim enzimlerini (lipaz, amilaz, tripsin, kimotripsin vb.) ve özellikle vücuttaki şeker metabolizmasını düzenleyen insülin ve glukagon gibi bazı hormonları salgılamaktır ve yaşam için elzem bir organdır.
Normalde vücuttaki hücreler düzenli bir şekilde bölünerek çoğalır ve zamanı gelince de ölürler. Eğer hücreler kontrolsüz bir biçimde bölünmeye devam eder ve ihtiyac duyulmayan dokular oluşursa bu dokuların oluşturduğu kitlelere tümör denir. Vücutta oluşan tümörler habis (malign) veya selim (benign) karakterde olabilirler. Kanser terimi habis tümörler için kullanılır. Habis tümörler bulundukları bölgedeki yakın organlara ve kan ve lenf yoluyla da uzak organlara sıçrayabilirler ve bu durum metastaz olarak adlandırılır. Pankreas kanserinde de pankreas içindeki kanalları döşeyen hücrelerden kaynaklanan bir tümör gelişimi söz konusudur. Bu tür tümörler pankreasın ekzokrin tümörleri olarak adlandırılırlar. Bunlar arasında en sık görülenler pankreasın adenokanserleridir. Pankreasın daha nadir görülen tümör cinsleri pankreastaki hormon salgılayan hücrelerden kaynaklanan tümörler ve pankreasdaki kistik yapılardan kaynaklanan tümörledir. Bu guruptaki tümörler nöroendokrin tümörler ve kistadenokarsinomlar olarak adlandırılırlar ve nisbeten daha iyi bir gidiş gösterirler.
Pankreas kanseri ölümcül kanserler arasında 4. sırada yer alır. Görülme sıklığı 11/100.000 civarındadır. ABD de her yıl 42500 yeni vaka teşhis edilmekte ve 35000 kişi bu hastalık nedeniyle hayatını kaybetmektedir. Hastaların %80 i 60 yaş üzerindedir ve %50 sinde teşhis anında uzak metastaz bulunur. Erkeklerde kadınlara göre biraz daha sık görülür (RR: 1,3). Tanı ve tedavideki gelişmelere rağmen 30 yıl öncesi ile karşılaştırıldığında 1 yıllık yaşam oranı %15 den %21 e, 5 yıllık yaşam oranı ise %3 den %5 e kadar yükselebilmiştir.
Pankreas kanserinin değişik türleri bulunur;
– Duktal infiltran adenokarsinom (En sık görülen türdür, %85-90)
– Solid psödopapiller neoplazm (%3)
– İntraduktal papiller müsinöz neoplazm (%5)
– Nadir görülen türler : Pankreatoblastoma (%0,5), andiferansiye adenokarsinom, medüller karsinoma, müsinöz kistadenokarsinom, asiner hücreli karsinom vb.
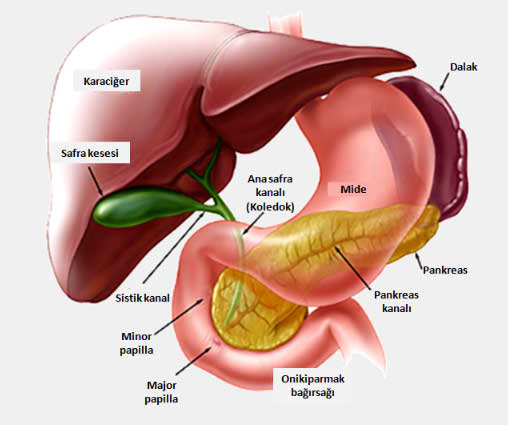
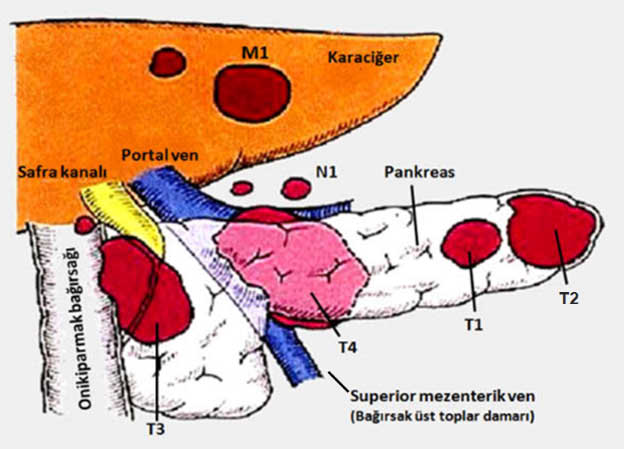
Pankreas ve komşu organların anatomisi
Pankreas kanserine ne neden olur?
Pankreas kanserinin nedeni kesin olarak bilinmekle birlikte hastalığın oluşmasına yol açtığı düşünülen bazı risk faktörleri belirlenmiştir ;
– 40 veya üzerinde olmak
– Erkek cinsiyet
– Sigara kullanmak
– Şeker hastalığı (Diyabet): 50 yaşından sonra ortaya çıkan şeker hastalığı olan hastaların %1 inde diyabet pankreas kanserinin erken bulgusu olabilir, gebelik diabeti olan kadınlarda pankreas kanseri riski artmıştır, RR:7,1).
– Kronik pankreatit (genellikle alkole bağlıdır): Herediter pankreatit olarak bilinen bir pankreatit türünde pankresa kanseri gelişme riski 53 kat artmıştır.
– Ailenin veya kişinin geçmişinde bazı kolon polip tiplerin veya kolon kanserin bulunması (FAP- Ailevi kalın barsak polipozisi, ailevi nonpolipöz kolon kanser sendromu vb.)
– Ailede pankreas kanseri varlığı: 1.derece akrabasında pankreas kanseri olanlarda yaşam boyunca pankreas kanseri görülme riski %4,7 dir, pankreas kanseri olan hasta hasta 60 yaşından genç ise bu oran %7,2 ye yükselir.
– Genetik yatkınlık (Pankreas kanserlerinin %7-10 undan sorumlu olduğu düşünülür)
– Yağ oranı yüksek gıdalarla beslenme (?): Aşırı kilo pankreas kanseri gelişimi bakımından risk faktörüdür.
Hastalığın belirtileri nelerdir?
Pankreas kanserinin erken evrelerinde genellikle hiçbir belirti görülmez. Hastalığa ait bulgular (semptomlar) ortaya çıktığında çoğunlukla tümör ileri bir evreye ulaşmış ve pankreas çevresindeki dokulara ulaşmıştır. Semptomlar, tümörün yerine ve büyüklüğüne bağlı olarak değişir ;
– İştahsızlık (%64)
– Nedeni açıklanamayan kilo kaybı (%66-84)
– Üst karında hissedilen ve bazen sırta vurabilen ağrı (%78-82)
– Sırt ağrısı (%48)
– Bulantı ve kilo kaybı (%50-86)
– Erken doyma (%62)
– Depresyon,halsizlik, çabuk yorulma
– Sarılık (%56-80) (Tümörün safra yollarını tıkaması sonucunda ortaya çıkar, göz aklarında sararma, idrarda koyulaşma ve dışkı renginde açılma olur)
– Diabet (Şeker hastalığ) (%97)
– Uyku bozukluğu (%54)
Yukarıdaki belirtiler pankreas kanseri dışında başka hastalıklarda da ortaya çıkabileceğinden bu tür yakınmaları olan kişiler bir doktora görünmelidirler.
Pankreas kanserinin nedenleri kesin olarak bilinmediğinden ve hastalık erken evrede herhangi bir belirti vermediğinden önlem almak zordur. Ailevi ya da genetik yatkınlıktan dolayı pankreas kanseri yönünden artmış bir riske sahipseniz doktorunuzun yardımıyla düzenli aralarla yapılacak tetkiklerle erken teşhis koymak mümkündür.
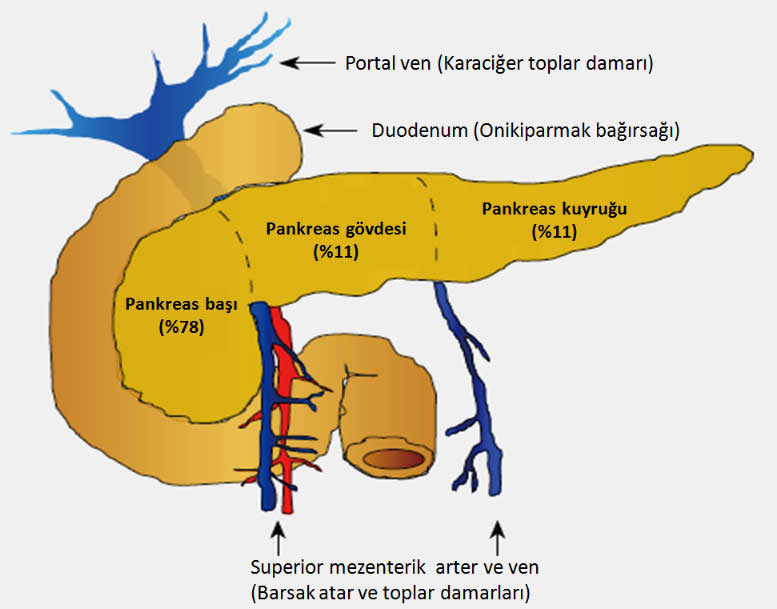
Pankreas kanserinde tümörün pankreastaki yerleşimi
TEŞHİS
Pankreas kanserinin teşhisinde doktorun bu hastalığın varlığından şüphelenmesi ve gerekli tetkikleri istemesi önemlidir. Bu amaçla aşağıdaki incelemeler yapılabilir;
Batın ultrasonografisi: İyi yapılmış bir ultrasonografi pankreas kanserinin erken teşhisinde yardımcıdır ve daha ileri düzeydeki incelemelerin yapılması konusunda karar verilmesine yardımcı olur. Ultrasonografinin iyi bir yanı radyasyon içermemesidir.
Ultrasonografi (US):
Duyarlılığı %48-89, özgüllüğü %40-90 arasında değişebilen, noninvaziv ve ucuz bir görüntüleme yöntemidir. 1cm den küçük tümörlerin ancak %50 si ultrasonografiyle tesbit edilebilirken 3cm den büyük tümörlerde yöntemin duyarlılığı %95 e yükselmektedir. Renkli Doppler ve iv kontrast US yöntemlerinin kullanıma girmesiyle tümöre komşu damarların tutulumu ve lezyonun vaskülaritesi (damarlanması) hakkında daha ayrıntılı bilgi elde edilebilmektedir. US pankreas kanserinde rezektabilitenin değerlendirilmesinde (tümörün cerrahi olarak çıkarılabilirliği) vakaların ancak %55 inde doğru sonuç verebildiğinden başka görüntüleme yöntemleriyle kombine edilmelidir. US de cihazın özellikleri yanında radyoluğun tecrübesi de yöntemin duyarlılığını etkileyen önemli bir faktördür.
Bilgisayarlı tomografi (BT):
Karın içerisindeki yapıların ve özellikle pankreasın daha ayrıntılı bir şekilde ve ince kesitler halinde incelenmesini sağlar. Radyasyon içermesi ve nisbeten pahalı oluşu dezavantaj oluşturmakla birlikte pankreas tümörü varlığından şüphelenildiğinde mutlaka yapılması gereken bir inceleme yöntemidir. 2cm den küçük kitlelerin saptanmasındaki duyarlılığı %77, özgüllüğü %100 dür. Rezektabilitenin tahminindeki doğruluğu %73, unrezktabilitedeki pozitif ömgörü değeri ise %90 dır. Son yıllarda 1-3mm lik çok ince kesitlerle tarama yapabilen MDCT nin kullanılmasıyla (Multi detector CT scanner) tümörün rezektabilitesi hakkında daha doğru karar verilmesi mümkün olmaktadır (Negatif öngörü değeri %87 vs %79).
Manyetik rezonan görüntüleme (MRI, magnetic resonance imaging):
Manyetik dalgalar yardımı ile karın içindeki yapılar BT dekine benzer bir şekilde incelenir. Radyasyon içememesi önemli bir üstünlüğüdür. Pankreas kanserinin evrelenmesinde BT ye üstündür (%100 vs %94). MRI ile birlikte MRCP (magnetic resonance cholangiopancretography) kullanımı benibn ve malign lezyon ayrımında yöntemin duyarlılığını ve özgüllüğünü artırır.
EUS (Endoskopik ultrasonografi):
EUS yönteminde endoskopun ucuna adapte edilmiş bir ultrasonografi probu ile barsak içinden ultrasonografi yapılarak tümörün saptanması, evrelemesi ve doku örneği alınması mümkün olmaktadır (Bkz EUS). Hastalığın lokal evrelemesinde BT ye göre daha duyarlı bir yöntemdir (%67 vs %41). Lenf nodu tutulumunun (%44 vs %47) ve rezektabilitenin (%68 vs %64) gösterilmesinde BT ile aynı duyarlılığa sahiptir. Portal ve splenik ven tutulumunun gösterilmesinde %90 gibi yüksek bir duyarlılığa sahipken SMA (superior mezenterik arter, bağırsak atar damarı) ve SMV (superior mezenterik ven, bağırsak toplar damarı) tutulumunun gösterilmesindeki duyarlılığı düşüktür (%50) (Negatif öngürü değeri %82). IV kontrast kullanılarak yapılan EUS daha yüksek duyarlılığa sahiptir (contrast enhenced EUS).
ERCP (Endoscopic retrograde cholangiopancreatography):
Endoskopik yöntemle pankreas kanalına kontrast madde verilerek pankreas kanalı görüntülenir. ERCP teşhisten çok pankreastaki tümörün safra yollarına bası yaparak tıkaması sonrasında oluşan sarılığın tedavi edilmesi amacıyla kullanılan bir yöntemdir (Bkz. Endoskopi- ERCP).
PET CT (Positron emission tomography):
Damar yoluyla verilen radyoaktif maddenin (F-2fluoro-2-deoxy-D-glucose – FDG) tümör dokusu tarafından tutulmasıyla tümörün görüntülenmesi esasına dayanan bir testtir. Yeni geliştirilen PET cihazları 7mm çapındaki küçük pankreas kanserlerini ve metastazları gösterebilmektedir. 1cm den küçük pankreas tümörlerinin (%92 vs %88) ve kemik metastazlarının (%100 vs %12) gösterilmesindeki duyarlılığı BT ye üstündür. Bununla birlikte, vasküler invazyonun (damarsal tutulum), paraaortik lenf nodu tutulumunun (aorta komşu lenf nodları) , peritoneal yayılımın (karın zarı tutulumu) ve karaciğer metastazlarınının gösterilmesinde duyarlılığı CT ye göre daha düşüktür (sırasıyla; %22 vs %100, %57 vs %78, %42 vs %57 ve %52 vs %73). PET, tümörün teşhisi yanında tedaviye alınan cevabın değerlendirilmesinde de kullanılır. Bu amala SUV değeri kullanılır [standardized uptake value = Doku konsantrasyonu (miliküri/g) / Enjeksiyon dozu (miliküri) / Vücut ağırlığı (g)]. Metastatik hastalığı olan pankreas kanserli vakalarda SUV değeri yüksektir (>6) ve prognoz tahmininde yardımcıdır.
PET pankreas kanseri ve pankreatit ayrımında yardımcı olabilir. FDG nin diffüz tutulumu pankreatitte pankreas kanserine göre daha sık görülen bir bulgudur (%53 vs %3). Hayvan çalışmalarında pankreas kanserlerinin erken evrede saptanmasında ve pankreatit ayrımında C-acetate-PET in FDG-PET e göre daha duyarlı olduğu görülmüştür.
Tümör dokusundan örnek alınması (Biyopsi):
Pankreasta bir kitle tesbit edildiğinde kesin tanı ve tümör cinsinin anlaşılması amacıyla doku örneği alınması gerekir. Bu aynı zamanda daha sonra uygulanacak olan ilaç tedavisinin seçiminde de yardımcı olur.
Kan testleri:
Pankreas kanserinde de diğer bazı kanser çeşitlerinde olduğu gibi kanda tümör belirteçleri (tumor marker) olarak adlandırılan birtakım maddelerin arttığı saptanabilir. Bu maddeler genellikle tümörün kendisi tarafından oluşturulabildiği gibi bazen vücut tarafından da oluşturulabilir.
Pankreas kanserinde yükselen tümör belirteçleri CA19-9 (Carcinom antigen 19-9) ve CEA (carcino embrionic antigen) dir. Bu maddeler pankreas kanseri için spesifik olmayıp sindirim sisteminin diğer kanserlerinde, safra yolları hastalıklarında ve pankreasın bazı selim hastalıklarında da yüksek bulunabilir. Tümör belirteçleri tanıdan çok tedaviye alınan cevabın değerlendirilmesi ve hastanın tedavi sonrasında izlenmesi amacıyla kullanılırlar. CA19-9 düzeyi 370U/ml nin altında olan hastalarda yaşam süresi, daha yüksek değerlere sahip hastalara göre daha uzundur (9,6 ay vs 4,4 ay). CA 19-9 seviyesi 200U/ml nin altında olan hastalarda hayatta kalım süresi daha uzun bulunmuştur (22 ay vs 8ay ). Sarılık gelişen hastalarda kanda yükselen bilüribin nedeniyle CA19-9 düzeyi yanlış olarak olduğundan daha yüksek çıkabilir. Bu etkileşim CEA de görülmez. CEA pankreas kanseri için daha az duyarlı bir test olup özellikle pankreas öz suyunda ölçüldüğünde daha anlamlı sonuç verebilir. Pankreas öz suyundaki CEA düzeyi ölçümü pankreas kanserlerinin erken teşhisinde yardımcı olabilen bir testtir (>50mg/ml).
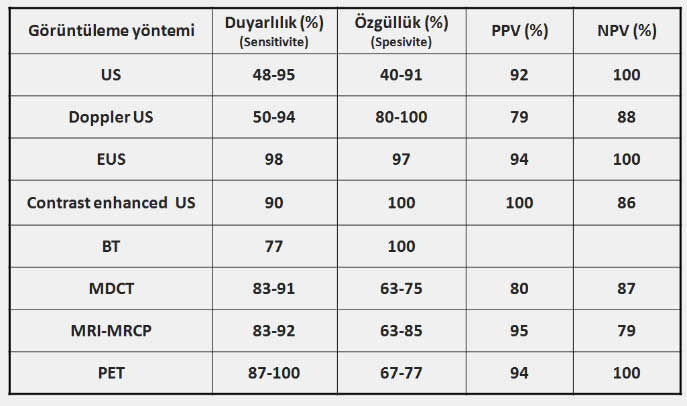
Pankreas kanseri teşhsinde ve evrelemesinde kullanılan görüntüleme yöntemlerinin duyarlılık ve özgüllükleri (PPV: pozitif kestirim değeri, NPV: Negatif kestirim değeri) (1)
EVRELEME
Pankreas kanseri tedavisinde uygun yaklaşımı saptamak amacıyla öncelikle tümör evrelemesinin yapılması (Tümörün ne kadar büyüdüğünün ve komşu ve uzak organlara yayılım derecesinin saptanması) gerekir. Çünkü pankreas kanser tedavisinde uygulanacak tedavi yöntemleri kanserin evresine bağlı olarak değişir. Tümörün çölyak arter, superior mezenterik arter (SMA) ve hepatik arteri 180′ den fazla çevreleyecek şekilde yayılımı veya bu bölgedeki bağırsak toplar damarlarında masif tromboz oluşması halinde cerrahi tedavi uygulanamaz. Portal ven ve superior mezenterik venin tromboz oluşmadan tutulumu cerrahi rezeksiyona engel teşkil etmez. Bu nedenle gerektiğinde birden fazla görüntüleme yöntemi kullanılarak doğru evreleme yapılması gerekir. Bazı otörler kritik vakalarda laparoskopik evreleme yapılmasını tavsiye ederler (karın içine teleskopik bir aletle bakılması). Araştırmalar, görüntüleme yöntemlerinde rezektabl kabul edilerek cerrahiye verilen vakaların %20-48 inin ameliyat sırasında aslında anrezektabl bulunabileceğini göstermiştir.
Evre 1: Tümör pankreas dışına sıçramamıştır
Evre 2: Tümör pankreasın sınırları dışına çıkmış, ana safra kanalına ve oniki parmak barsağı duvarına ve pankresa komşu lenf bezlerine sıçramıştır.
Evre 3: Tümör pankreas dışına, yanındaki mide, kalın barsak ve dalak gibi organlara ve lenf düğümlerine sıçramış, pankreasın etrafındaki büyük kan damarlarına da yayılmıştır.
Evre 4: Tümör karaciğer gibi uzak organlara sıçramıştır.
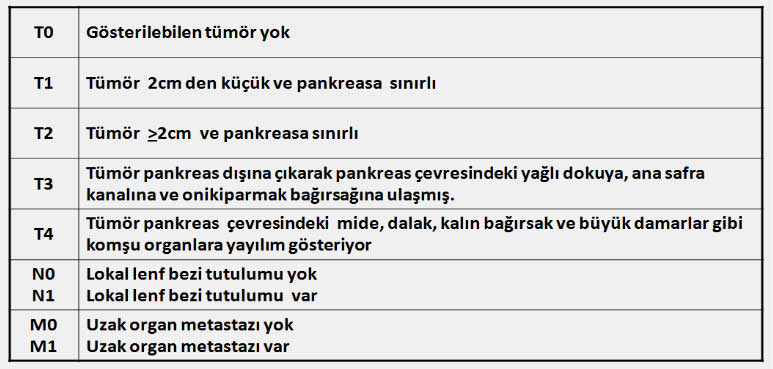
Pankreas kanserinde TNM evreleme sistemi (T: Tümör, N:Lenf nodu, M:Metastaz)
Pankreas kanserinde TNM evreleme sistemi
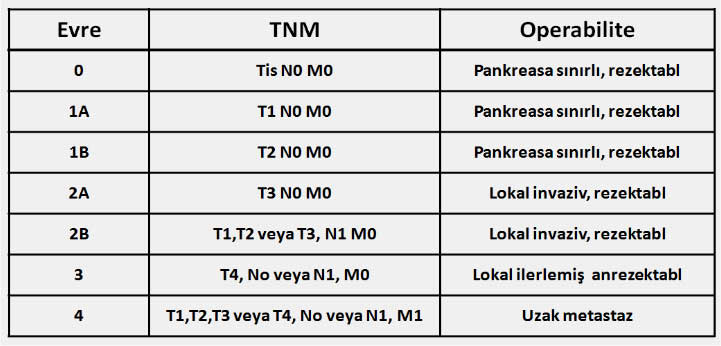
Pankreas kanserinde evreleme, TNM sistemi ve operabilite (rezektabilite)
Bu sınıflamaya göre pankreas kanseri klinik olarak 3 kategoriye ayrılabilir;
1.Kategori: Pankreasa lokalize kanseri olan hastalar (Tis-T2) (Görülme sıklığı %8, beş yıllık hayatta kalım %22)
2.Kategori: Lokal invaziv- regional lenf nodu tutulumu olan hastalar (T3) (Görülme sıklığı %26, beş yıllık hayatta kalım %9)
3-Kategori: Unrezektabl (cerrahi olarak çıkarılamayan) tümörü (T4) ve/ veya uzak metastazı olan hastalar (Görülme sıklığı %53, beş yıllık hayatta kalım %2)
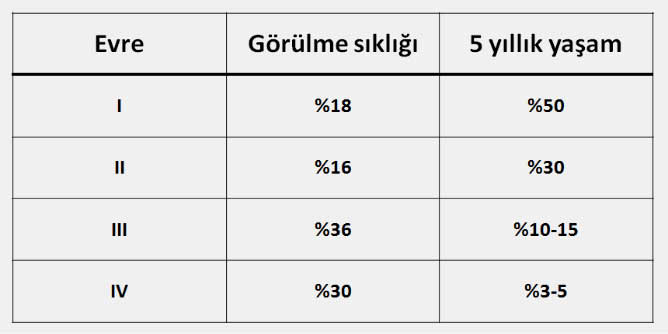
Pankreas kanserinde hastalığın evresine göre beklenen yaşam süresi
TEDAVİ
Cerrahi tedavi:
Pankreas kanseri olgularının ancak %20 si teşhis anında radikal cerrahi tedavi adayı olabilmektedir. Pankreasın gövde ve kuyruk kısmında yerleşim gösteren tümörler geç belirti verdiklrinden teşhis anında hastalık genellikle ileri evrededir ve rezektabl değildir.Tümörün çölyak arter, superior mezenterik arter (SMA) ve hepatik arteri 180′ den fazla çevreleyecek şekilde yayılımı veya bu bölgedeki bağırsak toplar damarlarında masif tromboz oluşması halinde cerrahi tedavi uygulanamaz. Portal ven ve superior mezenterik venin tromboz oluşmadan tutulumu cerrahi rezeksiyona engel teşkil etmez. Cerrahi tedavide kanserli tümör, tümöre komşu dokular ve yakındaki lenf düğümleri çıkarılır (Pankreatikoduodenektomi, PD). Whipple ameliyatı olarak adlandırılan cerrahi yöntemde pankreas baş kısmında yerleşik tümörlerde pankreasın büyük bir kısmı, midenin bir kısmı, onikiparmak barsağı ve etrafındaki dokular alınır. Son yıllarda uygulanmakta olan yöntem pilor koruyucu PD yöntemidir (PPPD). Bu yöntemde operasyon süresi daha kısa olup kan kaybı daha azdır. PPPD de ameliyat sonrasında ortaya çıkabilecek sindirim sistemi yakınmaları klasik PD ye göre daha az görülür ve cerrahi sonrasında gerektiğinde endoskopik olarak safra yollarına ulaşım daha kolaydır. Semptom süresi (sarılık ve ağrı) 40 günden uzun, CA19-9 seviyesi >200U/ml olan ve histolojik olarak G3-G4 evresi saptanan hastalarda ameliyat öncesi evrelemede hastalık rezektabl olsada prognoz kötüdür.Pankreasın kuyruk kısmında yerleşim gösteren erken evredeki tümörler laparoskopik rezeksiyonla çıkarılabilirler. Pankreasın tümüyle çıkarılması (total pankreatektomi) kronik pankreatit, multifokal adacık hücre tümörü veya diffüz IPMN (bkz. pankreas kistleri) olan vakalarda uygulanır.
Bazen asıl tümör kitlesi çıkarılamasa da kanserin yol açtığı kusma, sarılık vb. durumların ortadan kaldırılması için cerrahi tedavi uygulanması gerekebilir. Tümörin safra yollarını tıkamasına bağlı olarak ileri derecede sarılığı olan hastalarda ameliyat öncesinde endoskopik (ERCP) ve/veya radyolojik (PTK) yöntemlerle safra yolları drene edilmelidir (Biliyer dekompresyon). Sarılığı hafif olan vakalarda bu işlemler yapılmadan hasta ameliyata alınabilir. Ameliyat öncesinde safra yollarına uygulanacak gereksiz girişimler safra yollarında enfeksiyon gelişme riskini artırır. Cerrahi tedavi öncesinde kemoterapi ve radyoterapi uygulanacak olan sarılıklı vakalarda işlem öncesinde yukarıdaki yöntemlerden biri kullanılarak mutlaka safra yolu drenajı sağlanmalıdır.
Radyoterapi:
Radyasyon ile tümör hücrelerinin öldürülmesine ve tümörün küçültülmesine çalışılır. Cerrahi girişim öncesinde veya sonrasında uygulanabilir. Vücut dışından uygulanabileceği gibi bazen tümör yakınına koyulan radyoaktif çekirdeklerle vücut içinden de yapılabilir. Radyoterapi hastalığın lokal kontrolüne fayda sağlar. Pankreas baş kısmında yerleşim gösteren kanserlerde 5-FU ile birlikte uygulanan radyoterapi (kemoradyoterapi) sonrasında Gemcitabine ile tedaviye devam şeklinde bir yaklaşım bazı kliniklerde standart tedavi yöntemi olmuştur.
Kemoterapi :
Kemoterapide verilen kemoterapötik ilaçlarla kanser hücrelerinin öldürülmesi veya çoğalımlarının durdurulmasına çalışılır. Cerrahi tedavi şansı olan hastalarda kemoterapi cerrahi tedavi öncesinde veya sonrasında verilebilir (Neoadjuan ve adjuvan tedavi). Cerrahi tedavi şansı olmayan hastalarda günümüzde tek geçerli tedavi şansı kemoterapidir. Kemoterapi ve radyoterapi birlikte uygulandığında daha iyi sonuç alınabilir. Kemoterapide etkili olabildiği gösterilmiş olan ajanlar 5-FU (Fluorouracil), Leucovorin ve Gemcitabine dir. Tek başına 5-FU veilen vakalarda tedaviye cevap alınma oranı %8-15 ilen 5-FU + leucovorin uygulanmasıyla bu oran %26 ya yükselir. Cerrahi tedaci sonrasında kemoterapi ve radyoterapinin birlikte uygulanması (adjuan kemoradyoterapi) yaşam süresini uzatabilmektedir [ 2 ve 5 yıllık hayatta kalım %43 vs %18 ve %19 vs %0, GITSG (Gastrointesinal Tumor Study Group) çalışması].
Kemoterapi ve radyoterapinin cerrahi tedavi öncesinde uygulanması (neoadjuvan tedavi) anrezektabl olguların 1/3 inde rezektabilite şansı yaratabilmektedir. Rezektabl tümörlerde neoadjuvan tedavi uygulaması yaşam süresine olumlu bir katkı sağlamaz.
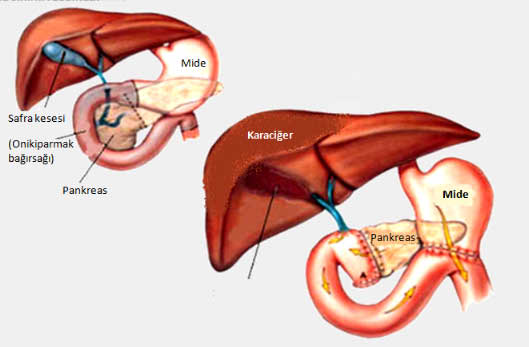
Pankreas kanserinde cerrahi tedavi (Whipple prosedürü)
Biyolojik Tedavi (Biyoterapi – İmmunoterapi ):
İmmunoterapi olarak da bilinen biyolojik terapide, bağışıklık sistemi ( vücudun kendi koruma mekanizmaları) kanserle savaşır. Bağışıklık sistemin yeterli çalışmaması durumunda kanser oluşumunun kolaylaştığı bilinmektedir. Biyoterapi ile vücudun bağışıklık sistemi onarılır, uyarılır ya da kuvvetlendirilir. Biyoterapi tek başına uygulanabileceği gibi cerrahi tedavi, radyoterapi ve kemoterapi ile beraber de uygulanabilir. Bu şekilde tedaviye bağlı yan etkilerin azalması da sağlanmış olur.
Biyoterapi ile,
– Kanser oluşum süreci durdurulur, kontrol edilir ya da bastırılır
– Kanser hücreleri bağışıklık sistemimiz tarafından daha kolay farkedilir hale getirilir.
– T-hücreleri, NK-hücreleri ve makrofajları gibi bağışıklık sistemi hücrelerinin öldürme gücü artırılır
– Normal bir hücreyi kanser hücresine dönüştüren sürec durdurulur ya da geri döndürülür
– Vücudun, tedavi süreci içinde ölen ya da hasarlanan hücrelerinin yerine yeni hücre üretmesi hızlandırılır.
– Kanser hücrelerinin vücudun başka yerlerine sıçraması engellenir.
Biyolojik tedavi yöntemleri:
İnterferonlar
İnterferonlar vücut tarafından enfeksiyon durumunda üretilir. İnterferonlar hem enfeksiyon oluşturan yabancı maddelerle hem de kanser hücreleri ile savaşır.
Monoklonal Antikorlar
Vücuttaki her hücrenin yüzeyinde kendini tanıtan proteinler vardır. Kanser hücrelerinde değişeime uğrayarak farklılaşmış olan bu proteinler bağışıklık sisteminin uyarılmasına yol açar. Bu proteinler kanser antijenleridir ve vücut onlara karşı antikor olarak adlandırılan başka proteinler üretir. Bir tane ana antikordan aynı antijene karşı sayılarca antikor klonu üretildiğinden monoklonal diye adlandırılmaktadır. Bu tedavide kanser hücrelerinden örnek alınırak kanser hücrelerinin yüzeyinde bulunan antijenler saptanır. Sonra bu antijenlere bağlanıp antijenin üzerinde yer aldığı hücreyi öldürecek olan antikor üretilir. Bu yöntem ile üretilen antikorlar kanser hücrelerini öldürmek için tek başına kullanılabildiği gibi tedavi veya tanıda gerekli olan maddelerin kanser hücrelerine taşınmasında da kullanılabilirler. Monoklonal antikorlar ile kemoterapötik ajanların doğruca tümör hücrelerine taşınması mümkün olabilmektedir. Bu şekilde ilacın sağlıklı dokulara zarar verme oranı da azalır. Yüksek konsantrasyonda kullanılabilindiğinden etkinliği konvansiyonel kemoterapiden daha yüksektir ve yan etkileri de daha azdır. Monoklonal antikorların kanser tedavisinde kullanımı yenidir ve sadece kemoterapiye dirençli vakalarda uygulanmaktadır. Günümüzde pankreas kanserinde kullanılan monoklonal antikor ‘setuksimab’ dır. Bu ilacın içerdiği antikor kanser hücresine bağlanarak hücrenin anormal çoğalmasını ve saldırgan karakter kazanmasını engeller. Tedavinin etkinliğini değerlendirmeye yönelik çalışmalar halen sürmektedir.
Monoklonal antikorlar tanısal amacla da kullanılabilir. Antikorla birleştirilen radyoaktif maddelerin kanser hücelerine bağlanmasıyla diğer yöntemler ile görüntülenemeyen kanser hücrelerinin ve metaztazların görüntülenmesini sağlanır.
İnterlökinler
İnterlökinler, vücudun lenfositlerini (bir çeşit akyuvar) aktive eder. Yani bağışıklık sistemi için önemli olan beyaz kan hücrelerinin (akyuvarlar) coğalımını ve çalışmalarını uyarırlar. Bu şekilde vücut direncinde artma sağlanır. Örneğin, IL-2, tümör hücrelerini öldüren hücreleri aktifleştirir ve bağışıklık fonksiyonun kuvvetlenmesine katkıda bulunur.
Palyatif tedavi yöntemleri:
Pankreas kanserinde lokal invazyon ve uzak metastaz nedeniyle olguların %80-90 ında ilk teşhis anında anrezektabl (cerrahi olarak çıkarılamayan) bir tümör sözkonusudur. Pankreas başı ve gövdesinde yerleşim gösteren tümörü olan bu tür vakalarda ortalama yaşam süresi 7 aydır. Pankreas kuyruğunda yerleşim gösteren tümörü olan olgularda bu süre daha da kısadır (ortalama 3 ay). Pankreas kanserinde büyüyen tümöre bağlı olarak ortaya çıkan mide çıkış darlığı, sarılık, ağrı,kanama ve kilo kaybı gibi semptomlar hastanın ve hasta yakınlarının yaşam kalitesini belirgin ölçüde bozabilir.
Mide çıkış darlığı tümörün onikiparmak barsağına invazyonu sonrasında oluşur ve inatçı bulantı ve kusmalarla kendini belli eder. Bu vakalarda endoskopik stenting (endoskopla daralan bağırsak bölgesine veya mide çıkışına bir stent yerleştirilmesi) veya gastroenterostomiyle (ameliyatla ince bağırsağın mideye bağlanması) kusmaların önüne geçmek mümkün olabilir.
Sarılık pankreas başında yerleşim gösteren tümörün safra yolunu sıkıştırması veya invazyonu sonrasında ortaya çıkar. Bu vakalarda ERCP veya PTK gibi yöntemlerle daralmış safra yoluna bir stent yerleştirilerek sarılık ve kaşıntının hafiflemesi sağlanır. Karaciğerde yaygın metastaza bağlı sarılığı olan vakalarda stenting fayda sağlamaz. Tümörün onikiparmak bağırsağını invaze ettiği vakalarda bazen şiddetli olabilen sindirim sistemi kanamaları olabilir. Bu hastalarda radyolojik yöntemlerle tümörü besleyen atardamarların tıkanmasıyla kanama durdurulabilir.
Pankreas kanserinde görülen karın ve sırt ağrısı ağız yoluyla veya enjeksiyonla alınan ağrı kesicilerle bir dereceye kadar dindirilebilir. Ancak hastalığın ilerleyen evrelerinde ağrıları şiddetlenen hastalarda pankreasa yakın bölgede bulunan sinir ganglionları (celiac plexus) alkol enjeksiyonu ile paralize edilerek ağrı palyasyonu sağlanır. Bu amaçla endosonografik veya radyolojik kontrol altında sinir gangliaonlarının olduğu bölgeye %50-100 lük alkol enjekte edilir. Yöntem ameliyat sırasında da uygulanabilir. Hastaların %70-95 inde bu tedaviye yanıt alınır.
Kaynaklar
1) Sharma C, Eltawil KM, Renfrew PD, Walsh MJ, Molinari M.Advances in diagnosis, treatment and palliation of pancreatic carcinoma: 1990-2010.World J Gastroenterol. 2011;17(7):867-97.
2) Ouaïssi M, Giger U, Louis G, Sielezneff I, Farges O, Sastre B.Ductal adenocarcinoma of the pancreatic head: a focus on current diagnostic and surgical concepts.World J Gastroenterol. 2012;18:3058-69.
3) Herreros-Villanueva M, Hijona E, Cosme A, Bujanda L.Adjuvant and neoadjuvant treatment in pancreatic cancer.World J Gastroenterol. 2012;18:1565-72.
4) Shin EJ, Canto MI.Pancreatic cancer screening.Gastroenterol Clin North Am. 2012;41:143-57.
5) Koido S, Homma S, Takahara A, Namiki Y, Tsukinaga S, Mitobe J, Odahara S, Yukawa T, Matsudaira H, Nagatsuma K, Uchiyama K, Satoh K, Ito M, Komita H, Arakawa H, Ohkusa T, Gong J, Tajiri H.Current immunotherapeutic approaches in pancreatic cancer.Clin Dev Immunol. 2011:267539.doi:10.1155/2011/267539.