Reflü komplikasyonları nelerdir?
GÖRH nın komplikasyonları aşağıdaki tabloda görülmektedir. Peptik striktür hastaların %4-20 sinde (Ortalama %10) görülür.
Genellikle kardiyoözofagial bileşkede veya özefagusun 1/3 alt kısmında oluşur. Peptik striktürün başlıca belirtisi progresiv karakterde olan disfajidir ancak dar bölgede özefagusun çapı 12mm nin altına inmedikçe semptom vermez. Özefagus pasaj grafisi ve endoskopi ile tanı koyulur. Ayırıcı tanıda distal özefagus veya kardia tümörleri düşünülmelidir. Medikal tedavi ile ödem ve inflamasyonun düzeltilmesinden sonra endoskopik balon dilatasyonu denenir. Bu tedaviye cevap vermeyen vakalarda dar bölgeye stent yerleştirilebilir veya cerrahi tedavi uygulanır. GÖR hastalarının %5 den az bir kısmında distal özefagusdaki özofajite ilave olarak bazen şiddetli kanamalara yol açabilen derin ülserler oluşabilir (Wolf ülserleri). Bu ülserler genellikle tıbbi tedavi ile düzelirler. Perforasyon oldukça nadirdir (<%1). GÖRH daki kanama daha çok gizli kan kaybı şeklindedir ve özellikle yaşlı hastalarda kronik demir eksikliği anemisi şeklinde ortaya çıkar. GÖRH kronik larenjit, astım, aspirasyon pnömonisi, atelektazi ve bronşiektazi gibi özefagus dışı komplikasyonlara yol açabilir ve bu durum tıbbi tedaviye cevap vermeyen hastalarda cerrahi tedavi için bir endikasyon oluşturur.
Gastroözofagial reflü hastalığının komplikasyonları Toplumda özefagus kanseri görülme sıklığı coğrafi bölgelere göre değişiklik göstermekle birlikte 1-6/100.000 civarındadır. Yapılan çalışmalar gastroözofagial reflü hastalığı varlığında yemek borusu kanseri görülme sıklığının bir miktar arttığını göstermekteyse de bu artış orta ve hafif şiddetteki reflü vakalarında fazla belirgin değildir. (Reflü şikayeti olmayanlarda %0,002, hafif ve orta şiddette reflüsü olanlarda %0,003-0,018, şiddetli reflüsü olanlarda %0,035). Pratikte bir hastada özefagus kanserinin özofajit, Barrett metaplazisi ve daha sonra kanser gelişimi şeklinde birbirini izleyen dönemlerden birinde yakalanması çok nadir olabilecek bir durumdur. Bugünkü bilgilerimiz, reflü hastalığında yemek borusu kanseri gelişme sıklığında hafif ancak ihmal edilebilir düzeyde bir artış olduğunu göstermektedir ve bu risk cerrahi tedavide görülebilecek ciddi komplikasyonların gelişme olasılığından (%0,5-1,5) belirgin ölçüde daha düşüktür (8,26).
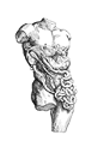
Kronik reflü sonrasında özefagusta oluşan darlığın radyolojik görünümü
Barrett metaplazisi
GÖRH nın şüphesiz ciddi ve sessiz bir komplikasyonu prekanseröz bir hastalık olan Barrett metaplazisinin gelişmesidir. Bilindiği gibi distal özofagusdaki çok katlı skuamöz epitelin yerini metaplazik kolumnar epitelin alması Barrett özofagusu olarak adlandırılır ve genellikle uzun süren GÖRH sonucudur. Uzun süreli aside maruz kalma sonucunda kolumnar epitel metaplazisinin gelişmesi aslında özofagus epitelinin zararlı etkenden (mide asidi) korunmasına yönelik bir adaptasyon mekanizması gibi görünmektedir. Bu metaplazik hücrelerin nereden geldiği sorusu halen cevaplanmış olmamakla birlikte mukozada bulunabilecek kök hücrelerden kaynaklanabileceği düşünülmektedir. Genel olarak endoskopi yapılanlarda Barrett metaplazisine rastlanma sıklığı %0.5-1, GÖRH nedeniyle endoskopi yapılanlarda rastlanma sıklığı ise %5-15 (ortalama %10) dir. Özofagusda peptik striktür varlığında bu oran %50 ye kadar çıkabilir. Özofagusa safra reflüsü varlığında da Barrett metaplazisi daha sık görülmektedir. Barrett özofagusu her yaşta görülebilmesine rağmen 40 yaş sonrasında görülme sıklığı artar. Barrett özofagusundaki metaplazik kolumnar epitelin üç tipi tanımlanmıştır;
1- Kavşak tipi (junctional) olarak adlandırılan ve kardia benzeri hücreler (Kardia tipi),
2- Mide fundusu epiteli benzeri hücreler (Fundik tip)
3- Paneth ve goblet hücreleri varlığı gösteren barsak tipi epitel (İntestinal tip).
Özofagusdaki metaplazik epitel 3 cm den kısa bir segmenti tuttuğunda kısa segment Barrett (short segment Barrett), 3cm den uzun bir segmenti tuttuğunda ise uzun segment Barrett metaplazisinden (long segment Barrett) bahsedilir. 1cm ve daha kısa Barrett metaplazisi genel olarak endoskopi yapılan insanların %10-15 inde görülebildiğinden GÖRH ile ilişkisi tartışmalıdır. Barrett meplazisinde metaplazik alanın tarifinde standart bir uygulama sağlanması amacıyla uygulanmaya başlanan daha yeni bir sınıflama sistemi reflü çalışma gurubu tarafından geliştirilmiş olan C&M Prag sınıflama sistemidir. (WGCO, Working Group for the Classification of Reflux Eesophagitis C&M Prague criteria). Bu sistemde, kolumnar epitelin distal özefagustaki maksimal (M, maximal lenght) ve sirküler tutulum gösteren bölgedeki yükseklikleri (C, circumferential lenght) ölçülerek Barrett metaplazisi sınıflandırılır. Bu sistemde adacık halindeki metaplazik alanlar ayrıca belirtilir (Şekil 13). Bazı hastalarda metaplazik segmentin uzunluğu yılda 0.5-1.5 cm kadar uzama gösterebilir.
Endoskopide Barrett özefagusu saptanan hastalarda yıllık adenokarsinom gelişme prevalansı %0,5 civarındadır. Bu oran Barrett metaplazisi olan hastalarda adenokarsinom gelişme riskinin genel popülasyona göre 30 ila 125 kat daha fazla olduğunu göstermektedir. Kanser gelişimi özellikle intestinal tipte metaplazide belirgindir. Uzun segment Barrett tutulumu olan, alkol ve sigara kullanan, yaşlı ve erkek hastalarda adenokarsinom gelişme riski artmıştır. Barrett epitelinden adenokanser gelişimi intestinal metaplazi-displazi ve insitu kanser evrelerini takiben ortaya çıkar. Displazi, şiddetine göre düşük veya yüksek dereceli displazi (low grade dysplasia-LGD , high grade dysplasia-HGD) ve kesinlik kazanmayan displazi (indefinite dysplasia) olmak üzere üç guruba ayrılır. Barrett metaplazisi olan hastaların 1/3 inde LGD, %5 inde de HGD ye rastlanır. 2 ve 5 yıl süre ile izlenen LGD li hastaların sırasıyla %10 ve %28 inde HGD ye dönüşüm görülür. LGD nin gerileyebildiğine dair bazı veriler olmakla birlikte sonuçlar çelişkilidir ve biyopsi alınma tekniği veya patolojik değerlendirmeden kaynaklanan sorunlar böyle bir sonuç alınmış olmasına yol açmış olabilir. ACG (American College of Gastroenterology) LGD li hastaların bir yıl ara ile endoskopi yapılarak takip edilmesini önermektedir. HGD de kansere dönüşüm sıklığı yıllık ortalama %5 civarındadır. 5 ve 7 yıl süre ile izlenen HGD li hastaların sırasıyla %15 ve %25 inde kanser geliştiği bildirilmiştir. Fokal HGD de %7 oranında kansere dönüşüm görülürken diffüz HGD de bu oran %36 ya çıkmaktadır. HGD li metaplazik mukoza düzgün yapıda olduğunda kansere dönmüşüm oranı %13 ken metaplazik mukoza nodüler yapıda olduğunda bu oran %63′e yükselmektedir. Bu sonuçlar metaplazik mukozanın nodüler yapıda olmasının ve diffüz HGD varlığının kansere dönüşüm riskini artırdığını göstermektedir. Düzgün yapıda mukozada HGD varlığında bir yıl sonunda ilerleme görülmediği taktirde izlemenin bir yıllık aralıklarla sürdürülebileceğini tavsiye eden yayınlar bulunmakla birlikte HGD nedeniyle rezeksiyon yapılan hastaların önemli bir bölümünde (%30-70) patolojik inceleme sırasında kanser saptanması nedeniyle günümüzde HGD saptanan hastaların insitukarsinom olarak kabul edilerek endoskopik veya cerrahi yöntemlerle tedavi edilmesi gerektiği görüşü hakimdir.
Barrett özefagusunda endoskopik takibin amacı kansere dönüşüm bulgularının ve gelişebilecek bir adenokanserin erken ve rezektabl dönemde yakalanabilmesidir. Belirgin endoskopik magnifikasyon sağlayan yeni endoskopik teknikler (NBI-narrow band imaging, high definition endoscopy, confocal endoscopy vb.) metaplazik alandaki şüpheli alanlardan yüksek doğrulukla biyopsi alınmasını sağlayabilmeleri bakımından giderek artan sıklıkta kullanılmaya başlanmıştır. Bu yöntemlerle mukozadaki villüslerde düzensiz yapı ve anormal vaskülarite görülmesi HGD varlığını %95 in üzerinde doğrulukla gösterebilmektedir. Barrett epitelinde kansere dönüşümün erken dönemde tesbit edilmesine yönelik başka yöntemler de mevcut olmakla birlikte bu yöntemler henüz rutin uygulama alanına geçmemiştir. 17. kromozomun kısa kolunda bulunan (17p) p53 geni mutasyonu ve sitometrik yöntemlerle saptanan anöploidi bu amaçla kullanılan yöntemler arasında sayılabilir. Mutasyona uğramış p53 geni yarılanma ömrü uzun olduğundan dokuda birikir ve immunhistokimyasal boyama yöntemleri ile kolayca gösterilebilir. Metaplazik epitelde LGD varlığında %0-10, HGD varlığında %57, adenokarsinom varlığında ise %100 oranında p53 pozitifliği bulunur. p53 negatif olan LGD li hastaların %0-15 inde kanser gelişirken p53 pozitif LGD li hastaların %30-78 inde kansere dönüşüm oluşmaktadır. Bu değişiklikler displazinin histolojik bulgularından önce ortaya çıkarlar ve kansere dönüşümün erken dönemde saptamasında yardımcı olurlar. Dokuda ornitin dekarboksilaz aktivitesi, CEA, mukus yapısındaki anormallikler, c-Ha-ras, c-erb-B gibi onkogenlerin aktivasyonu, hücre büyümesini, bölünmesini ve apoptozu düzenleyen proteinlerdeki değişiklikler (EGF, TGF-alfa, COX-2 vb.) kansere dönüşümü erken dönemde gösterilmesinde kullanılabilen diğer yöntemlerdir.
Aralıklı olarak asite (pH<4) ya meruz kalma Barrett epitelinde hücre proliferasyonunu belirgin ölçüde uyardığından kuvvetli asit supresyonu Barrett özefagusunda tedavinin temelini oluşturur. Barrett özefagusu olan hastalarda metaplazik epitelden alınan biyopsilerin sonucuna göre bir takip ve tedavi şekli uygulanır. Metaplazik epitelden 2 cm ara ile ve her dört kadrandan olmak üzere toplam 8 adet biyopsi alınmalıdır (Seattle protokolü). İnflamasyon ve özofajit bulguları olan hastalarda yüksek doz PPI tedavisiyle düzelme sağlandıktan sonra biyopsi alınmalıdır. Aktif inflamasyon bulguları varlığında displazinin değerlendirilmesi doğru değildir ve yanlış sonuçlara yol açabilir. Histopatolojik incelemede displazi yoksa hastanın PPI tedavisi ile 3 yılda bir endoskopik kontrolü yeterlidir. Hafif derecede displazi saptanan hastalarda PPI tedavisi altındayken ikinci endoskopi ilk yıl 6 ay ara ile tekrarlanmalı ve yine hafif displazi saptanması halinde hasta 1 yıl ara ile endoskopik kontrollere çağırılmalıdır. İki yıl üst üste displazi saptanmayan vakalarda izleme aralığı 3 yıla çıkarılabilir. Ağır derecede displazi saptanan hastalarda yoğun medikal tedavi sonrasındaki 3. ayda endoskopi tekrarlanmalı ve patolojik tanı başka bir patolog tarafından da doğrulandıktan sonra endoskopik veya cerrahi rezeksiyon yöntemlerinden biri uygulanmalıdır . Seçilecek yöntem metaplazik alanın genişliğine, yapısına (nodülarite vb.), hastanın yaşına, genel durumuna, komorbid hastalıkların varlığına, yöntemin uygulanabilirliğine ve hastanın seçimine göre belirlenmelidir. En iyi merkezlerde bile cerrahi rezeksiyonun mortalitesi %4-10, morbiditesi ise %35 civarındadır ve bu oranlar sıradan merkezlerde daha yüksek seviyelerdedir.
Cerrahiye kontrendikasyon teşkil eden durumların varlığında veya endoskopik tedavi için uygun olan vakalarda endoskopik mukozektomi, termal enerji (Lazer, elektrokoagülasyon, argon plazma koagülasyon ve radyofrekans enerji – HALO) ve fotodinamik tedavi yöntemleri denenebilir. Bunlar arasına en sık kullanılanlar fotodinamik tedavi yöntemleridir. Bu amaçla hastaya ‘hem’ biyosentezinde rol oynayan bir madde olan 5-aminolevulinic acid (5-ALA) veya bir hematoporfirin karışımı olan porfimer sodyum verildikten 4-6 saat sonra metaplazik epitele endoskopik olarak uygulanan laser daha önce epitelde biriken 5-ALA veya porfirini toksik forma dönüştürerek hücre ölümüne yol açar. Bu yöntemlerde başarı %40 ile %90 arasında değişebilen oranlarda bildirilmekle birlikte mortalite %5-8, morbidite ise %25 civarında olup striktür (%50), mediastinit, atrial fibrilasyon, perforasyon, plörezi, ciltte fotosensitivite gibi ciddi yan etkiler görülebilmektedir. Barrett metaplazisinin endoskopik tedavisinde umut verici termal yöntemlerden biri de argon plazma koagülasyonudur (HALO). Bu yöntemde özel bir balon veya aplikatör kullanılmak suretiyle geniş Barrett alanları endoskopik olarak bir veya iki seansta tedavi edilebilirken çok düşük seviyede komplikasyon oranları bildirilmektedir.
Barrett özofagusu tedavisinde umut verici görünen bir tedavi şekli de sekelektif siklooksijenaz inhibitörlerinin kullanımıdır (COX-2). Kolon poliplerinde ve kolon ve özofagus kanseri gibi bazı kanser türlerinde olduğu gibi Barrett epiteli hücreleri de aşırı miktarda COX-2 oluştururlar. Hayvan ve insanlar üzerinde yapılan çalışmalarda refecoxib veya cefecoxib gibi selektif COX-2 inhibitörlerinin kullanılması ile Barrett epitelinde hücre proliferasyonunun, displazi gelişiminin ve kansere dönüşümün yavaşlatılabileceği veya önlenebileceği yönünde umut verici sonuçlar alınmaktadır.
Barrett özefagusu nun endoskopik görünümü